
点击右上角![]() 微信好友
微信好友
 朋友圈
朋友圈

请使用浏览器分享功能进行分享

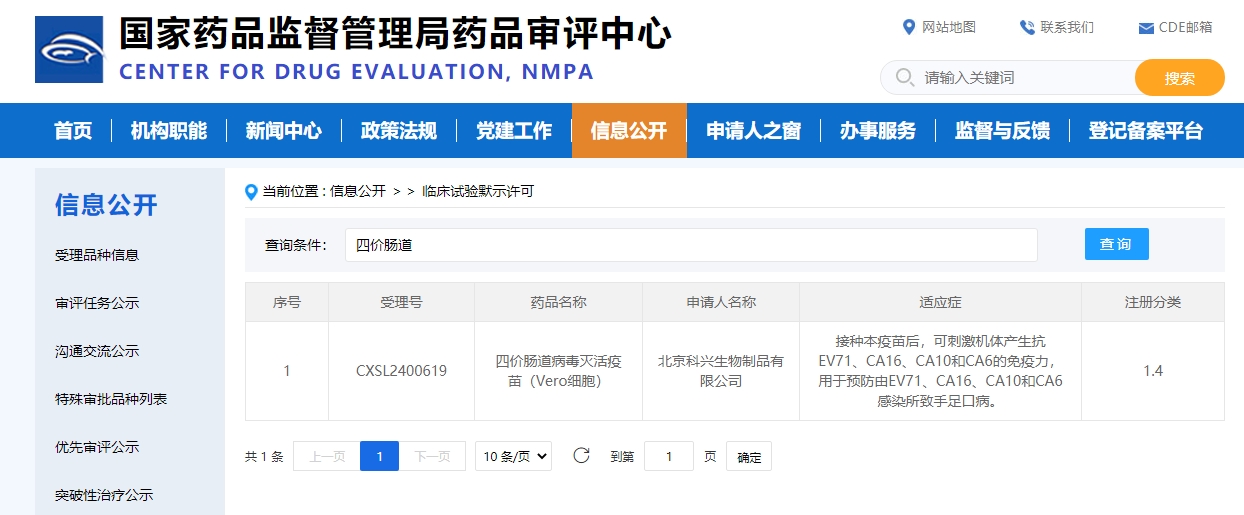
12月5日,国家药品监督管理局(NMPA)宣布,已正式批准SINOVAC科兴旗下北京科兴生物制品有限公司研制的四价肠道病毒灭活疫苗(Vero细胞)的临床试验申请。该疫苗用于预防由肠道病毒71型(EV71)、柯萨奇病毒16型(CA16)、柯萨奇病毒10型(CA10)、柯萨奇病毒6型(CA6)四种病毒感染所致手足口病。
手足口病作为一种常见的儿童传染病,其病原体多样,且各型别间的交叉免疫保护效果有限,因此,开发能够覆盖多种主流型别的多价疫苗成为防控该病的关键。近年来,SINOVAC科兴持续致力于多价手足口疫苗的研发。此前,其二价肠道病毒灭活疫苗已于2023年9月在国内率先进入临床研究阶段,并于今年9月成功完成Ⅱ期临床试验的揭盲工作。试验结果显示,该二价疫苗在6至71月龄的儿童群体中展现出了良好的安全性和免疫原性,为后续疫苗的研发奠定了坚实的基础。
随着EV71疫苗在国内的广泛应用,由EV71所致的手足口病发病和死亡占比大幅下降。然而,鉴于手足口病病原体的多样性,单一型别疫苗的防护作用有限,开发多价疫苗成为当务之急。
值得注意的是,手足口病目前尚无特异性的抗病毒药物,疫苗接种被视为预防该疾病的有效手段。INOVAC科兴在此领域已有一定的研究基础和市场经验。其自主研制的预防用生物制品1类新药益尔来福,自2015年在国内获批上市以来,已广泛应用于预防EV71引起的手足口病。今年9月,首批益尔来福已发往印尼,助力当地儿童手足口病防控。
SINOVAC科兴表示,公司始终以未被满足的公共卫生需求为己任。与合作伙伴紧密合作,加速推进二价和四价肠道病毒灭活疫苗的临床研究及上市进程,努力为全球儿童提供更多、更好的健康保护方案,共同守护儿童的健康成长。(张梦凡)
